欢迎访问西华大学-食品与生物工程学院!2024年06月12日11时53分56秒




近日,西华大学食品与生物工程学院发酵调味品科学与工程课题组在食品领域国际Top期刊Food Chemistry发表题为“Identifying and molecular mechanisms of novel antioxidant peptides from fermented broad bean paste: A combined insilico and invitro study”的研究论文。食品与生物工程学院林洪斌副教授为第一作者。

01.文章简介
本研究旨在研究发酵蚕豆瓣中抗氧化肽(FBBP)的抗氧化和细胞保护活性,并探讨其潜在的分子机制。通过肽组学和计算机生物信息学分析合成了7个新的抗氧化肽(VSRRFIYYL、SPAIPLP、PVPPPGG、KKDGYWWAKFK、LAWY、LGFMQF和LPGCP)。分子对接结果表明,这些肽与Keap1的关键氨基酸残基形成稳定的氢键和溶剂可及表面积,从而可能通过占据Keap1上的Nrf2结合位点来调控Keap1-Nrf2通路。这些肽同时具有较强的细胞抗氧化活性,可通过减少ROS和MDA的积累来保护HepG2细胞免受氧化损伤。本研究首次揭示了FBBP中抗氧化肽的分子机制,为FBBP的高值化利用提供了新的理论依据。
02.文章内容
蚕豆是一种富含蛋白质的作物,在发酵过程中,大量微生物的剧烈代谢活动将食品基质中的蛋白质转化为生物活性肽,包括抗氧化肽。在本研究中,最初使用超滤分离将WSP分成三个肽级分,测量每种组分的抗氧化性能。如图1a-c所示,WSP的结果在0.1至1.0 mg/mL浓度范围内呈剂量依赖性趋势,并随浓度增加而增加。在1.0mg/mL浓度下,DPPH、ABTS和OH-自由基的清除率分别为46.33±2.10%、44.22±0.96%和33.40±0.78%。经超滤分离后的U3自由基清除能力最强,表明随着分子量的降低,其抗氧化活性逐渐增强。一般而言,分子量越小的肽表现出越强的抗氧化活性。此外,大多数抗氧化肽在其N-末端(即V、L)含有疏水氨基酸,而Pro、His、Tyr、Trp、Cys在序列中。疏水性氨基酸的脂肪族侧链能够促进抗氧化肽与多不饱和脂肪酸之间的相互作用,以及与自由基的结合。此外,这些疏水性氨基酸可能更容易暴露在低分子量肽中,有助于肽-脂质相互作用,从而增强自由基的稳定性。
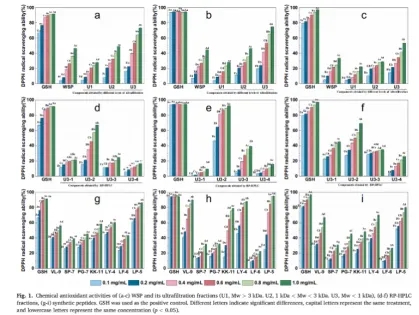
通过RP-HPLC将其分离为四个组分,各峰的抗氧化活性如图1d-f所示。U3-2对DPPH、ABTS和OH-自由基的清除能力显著高于其他3个组分(p < 0.05),在1.0mg/mL时,其清除率分别为67.03±0.27%、92.59±0.68%和69.25±2.76%。多肽的抗氧化能力还与芳香族氨基酸和含硫氨基酸的数量和位置有关,故收集了U3-2并用于随后的肽序列分析。计算机模拟方法已广泛应用于从食物衍生的蛋白质中发现新的生物活性肽,本研究采用UPLC-ESI-QTOF-MS/MS结合计算机模拟方法(包括Peptide Ranker、Toxin Pred、Pepdraw、Expasy compute pI/Mw分析和构效关系分析)对抗氧化活性最高的组分U3-2进行了鉴定。然而,目前关于抗氧化肽构效关系的研究还缺乏有效的信息。已报道含有芳香族或疏水性氨基酸的肽(Ile, Ala, Val, Phe, Asp, Tyr, Pro, Trp, Gly, Met and Leu)通过增强它们与脂质的相互作用或充当质子或氢供体来促进自由基清除活性。
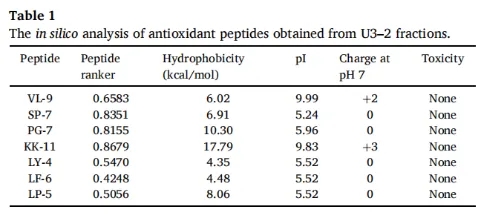
肽的物理化学性质和生物活性的计算机预测:使用计算机模拟工具对这些肽的5个指标进行了预测(表1)。根据肽的氨基酸序列,使用Peptide Ranker来预测潜在的生物活性,评分范围为0-1,评分越高意味着生物活性越强,该程序已广泛用于生物活性肽的预筛选。7种肽均表现出潜在的生物活性,肽排名得分>0.4。其中,KK-11的得分最高,这可能是由于该序列中重复氨基酸比例高和存在疏水性氨基酸所致。根据Pepdraw结果:KK-11的疏水性最高,为17.79kcal/mol,其次是PG-7(10.30kcal/mol)、LP-5(8.06kcal/mol),LY-4(4.35kcal/mol)的疏水性最低。这些结果与Peptide Ranker程序的预测一致。此外,这些肽的等电点(pI)在5.52和9.99之间,在pH 7时的净电荷为0、+2或+3。基于Toxin Pred预测得所有肽均无毒性,BIOPEP-UWM对这些多肽的氨基酸序列进行了检索,结果表明这些多肽均为首次发现。
如图1g-i所示为七种合成肽的体外抗氧化能力测定:均表现出较强的抗氧化效果,在0.1-1.0 mg/mL的浓度下显示出剂量依赖性增加趋势,表明计算机模拟方法可以有效地筛选生物活性肽。DPPH自由基清除活性已被用于评价天然提取物的抗氧化能力,由图1g可见,LP-5对DPPH自由基的清除率最高(86.40 ± 0.49%,1.0 mg/mL),但低于GSH,其次是LY-4(60.62±1.14%,1.0 mg/mL),而VL-9和KK-11在1.0 mg/mL时无显著差异(p > 0.05)。已有研究发现抗氧化肽WSAP与DPPH自由基之间存在氢键和疏水作用,其氨基酸残基能有效地与DPPH自由基分子相互作用,从而产生较强的DPPH自由基清除活性。
ABTS适合于测量蛋白质水解产物和肽的自由基清除活性,结果如图1h所示,LP-5在1.0 mg/mL时表现出最强的ABTS自由基清除能力,清除率为95.20±0.23%,当浓度超过0.8 mg/mL时与GSH无显著差异(p > 0.05)。LY-4、VL-9和KK-11(1.0mg/mL)对ABTS自由基的清除率分别为88.14±0.72%、90.09±1.14%和78.88±0.62%,抗氧化肽中的氨基酸残基可以清除与ABTS氢键和疏水相互作用的自由基,从而防止体内的氧化损伤。同样,TSSSLNMAVRGGLTR和STTVGLGISMRSASVR的潜在抗氧化活性是由S和T残基与自由基的相互作用引起的。LP-5序列中N端L以及Cys和Pro残基的存在显著增强了抗氧化能力,这主要归因于疏水氨基酸和芳香氨基酸的协同作用。另外,Tyr的酚羟基和Trp的吲哚基直接作为氢供体捕获自由基,从而清除自由基,这也解释了为什么LY-4具有较强的ABTS自由基清除能力。
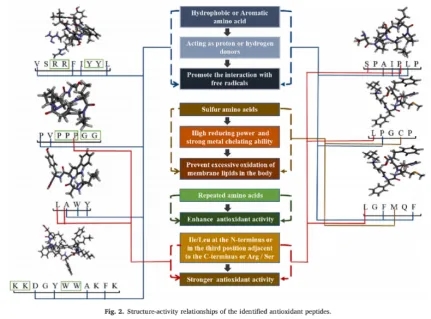
LP-5在1.0mg/mL时表现出最强的清除OH-自由基的能力,清除率为80.34±0.66%(图1i),其次是LY-4(70.41±0.65%)和VL-9(67.06±1.26%)。根据这些合成肽的构效关系(图2)和体外抗氧化能力(图1g-i),所有合成肽都具有理想的抗氧化能力。这些肽段可能是促进FBBP高抗氧化活性的活性因子之一,但其抗氧化机制和细胞保护活性尚需进一步研究证实。根据抗氧化能力测定的结果,选择LY-4、LP-5和VL-9作为代表性多肽,通过分子对接研究其抗氧化损伤的保护机制,同时进行细胞实验以评价其细胞保护作用。
在分子对接过程中,LY-4、LP-5和VL-9的对接能分别为-80.4859、-52.0058和-112.787kcal/mol。据报道,TX6(PubChem CID:121488089)具有与Keap1结合并激活Keap1-Nrf2途径的能力,是一种效果较好的抗氧化剂,与Keap 1之间的对接能为−25.45 kcal/mol。这些结果表明,三种抗氧化肽(LY-4、LP-5和VL-9)都能与Keap 1结合,且它们的结合复合物比TX6更稳定。其中,LP-5的自由基清除能力最强,这可能与该序列中Cys的存在有关。已经证实:含硫氨基酸Cys中的巯基易于被自由基氧化,从而保护细胞免受损伤。
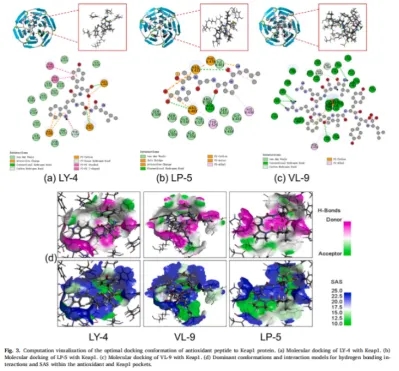
抗氧化肽和Keap 1之间具有最低的对接能,其3D结构图及相应的结合模式如图3所示,3种抗氧化肽均能很好地嵌入Keap 1的活性空腔中,形成稳定的构象。抗氧化剂与活性残基之间的结合力主要为碳氢、常规氢和静电吸引力,其次为盐桥、π-烷基、π-给体氢、π-阳离子和π-阴离子。此外,π-π T形和π-π堆叠参与结合。如图3(a)所示,Keap 1和LY-4中的Arg 483和Arg 415之间形成两个氢键,间距分别为2.22和2.23 nm,而残基Tyr 334和Arg 415形成π-供体氢和碳氢,Keap 1的Arg 483和Arg 415与LY-4形成两个吸引电荷相互作用。此外,两个π-阳离子和三个疏水相互作用(Tyr 572(π-π堆积),Tyr 525和Tyr 334(π-π T形)参与结合。由图3(B)可知,LP-5与Keap 1的Arg 415、Asn 414、Arg 483形成3个氢键, LP-5还与Keap 1的Arg 415、Phe 478和Arg 483残基形成四种电荷相互作用,与Phe 478、His 436和Tyr 525残基形成三种疏水相互作用(π-烷基)。VL-9可与Ile 416、Ser 431、Arg 483、Gly 433、Gly 364和Gly 603形成8个氢键,与Arg 415形成1个π-阳离子相互作用,距离为4.72 nm,与残基Phe 478形成1个疏水相互作用,其键距为4.87 nm(图3c)。
这些结果表明,氢键是这些力之间相互作用最重要且最强的因素,此外,残基Arg 415和Arg 483在抗氧化肽与Keap 1的结合中起着关键作用。
进一步分析了LY-4、VL-9和LP-5与Keap 1对接过程中存在的相互作用表面力。结果表明,表面力主要有六种,包括芳香相互作用、氢键作用、疏水性和溶剂可及表面、内插原子电荷和电离性,其中氢键作用和SAS是最强的表面力,因此,对这两种表面力进行了进一步的研究,详细情况如图3(d)所示。3种抗氧化肽与Keap 1蛋白活性结构域中的Arg、Tyr、Ile、Ser、Gly和Asn残基形成强氢键。根据图3:肽与Keap 1显示出强SAS,这可能与抗氧化肽和Keap 1之间存在相当大的范德华力有关。表明抗氧化肽与Keap 1的结合主要是通过氢键作用和SAS来实现的。总体而言,对接结果表明LY-4、LP-5和VL-9可能占据了Keap 1-Kelch结构域中Nrf 2的结合位点,从而抑制了Keap 1和Nr 2的相互作用,释放出游离的Nrf 2,促进了Nrf 2的积累,从而促进了抗氧化基的表达。
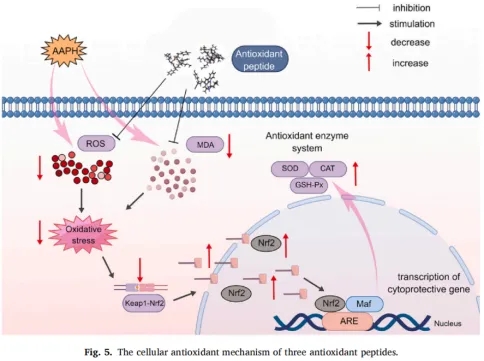
MDA由脂质过氧化作用产生,可与磷脂交联并被蛋白质中存在的巯基氧化,其含量变化被用作生物体中氧化应激的重要指标,并间接表征由ROS引起的对细胞的氧化损伤的强度。如图4(f)所示,与对照组(0.052 ± 0.020 nmol/mg蛋白)相比,AAPH诱导组的MDA含量(0.713 ± 0.026 nmol/mg蛋白)显著增加(p < 0.001)。抗氧化肽LY-4、LP-5和VL-9预处理显著降低了MDA的产生(p < 0.001)。同时,与AAPH诱导组相比,肽处理后细胞MDA水平的显著降低与ROS的降低一致,以上结果表明,LY-4、LP-5和VL-9三种抗氧化肽均能抑制ROS诱导的脂质过氧化反应,从而保护AAPH诱导的HepG 2细胞氧化损伤。一些研究已经报道,抗氧化肽可以通过增强抗氧化酶(即CAT、SOD和GSH-Px)的活性并降低ROS和MDA含量来保护细胞免受氧化损伤在本研究中,基于分子对接和细胞实验的结果,FBBP衍生的抗氧化肽(LY-4、LP-5和VL-9)的潜在作用机制总结于图5中。
My Diary 2024
03.文章总结
综上所述,基于计算机模拟和体外抗氧化活性分析,从FBBP中鉴定并合成了7个新的抗氧化肽,具有较强的抗氧化能力,其中LY-4、LP 5和VL-9具有最强的抗氧化和细胞保护作用。分子对接结果表明,3种抗氧化肽均能较容易地进入Keap 1的结合口袋,Arg 415和Arg 483残基在与Keap 1蛋白的结合中起关键作用,氢键和SAS是主要的相互作用表面力。这些抗氧化肽可能具有通过占据Nrf2和Keap1的结合位点来激活Keap1-Nrf2途径的潜力。此外,它们通过降低ROS和MDA水平对氧化损伤的HepG2细胞产生保护作用。这些结果有助于发现更多新的抗氧化肽,加深对抗氧化作用机制的认识,并为食品副产物的高效利用提供理论依据,但需要进一步的研究来确定其细胞活性和动物模型中的体内效应。
责编:唐紫薇
编审:唐洁
地址:中国·四川·成都·西华大学·第五教学楼D区
邮编:610039
电话:028-87720552
传真:028-87720552

官方微信